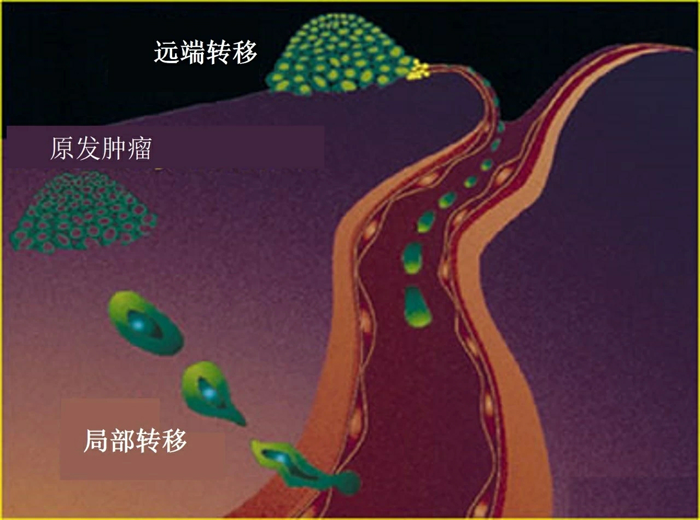
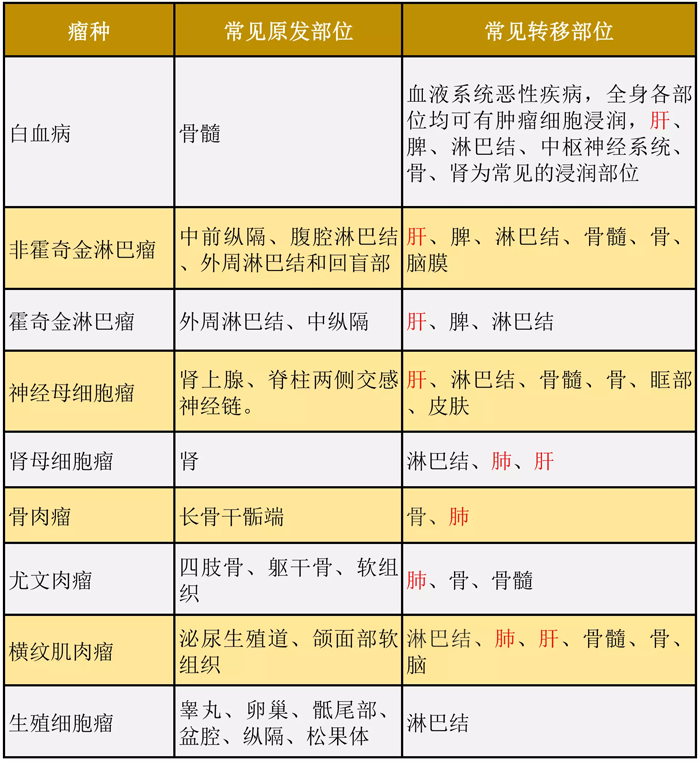
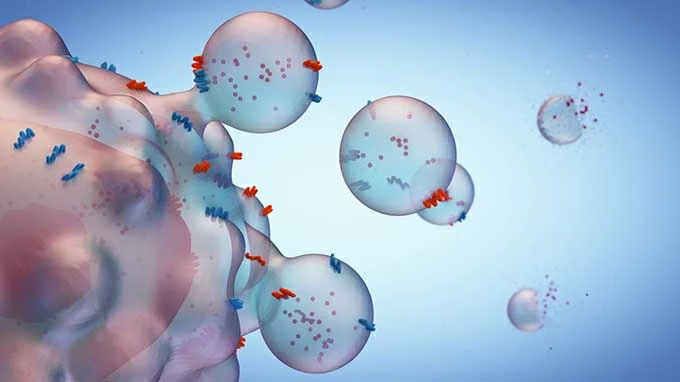
针对这一现象,英国医生Stephen Paget于1889年提出了“种子与土壤”的假设:他认为转移需要满足两个条件——流浪的癌细胞就像是“种子”,需要找到“肥沃的土壤”,也就是继发性肿瘤的器官内适合癌细胞生存的微环境,才能“茁壮成长”。
如同侦查小分队一般,外排体先行到达作为“土壤”的新器官,通过触发身体的炎症、自身免疫反应和促使血管形成等途径将自己融入新器官,为即将到达的“种子”癌细胞提供快速增殖的最优环境。
外排体身上有各种整联蛋白(integrins),它们可以给外排体贴上标签,以便癌细胞到了新的寄宿器官的时候能与那里的“门卫”对上暗号并顺利融合。
在这里,我们要曝光一下这些吃里扒外的“门卫”:它们有肺部的成纤维细胞(fibroblast) 和上皮细胞 (epithelial cell),肝巨噬细胞(Kupffer cell),以及脑内皮细胞(brain endothelial cell)。
而打断癌细胞与“叛徒门卫”的交流、阻断特异性癌细胞(或者他们特异的外排体)和被寄宿器官的良性细胞的融合,将是未来最有前景的治疗癌症转移的方案之一。
03
未来,我们将如何应对流浪杀手?
尽管我们对于转移癌细胞这些流浪杀手有了部分了解,然而要真正战胜这一行踪飘忽不定的对手,我们的作战技巧、武器装备以及对对手的充分了解仍有待提高。
因此,距离彻底战胜癌症的转移,显著提高患者的生存率,我们还需要在探索癌症的时代里,度过一段漫长和充满未知的时间。
首先,有能力离开家园到处“浪”的癌细胞,是那些束手就擒的癌细胞的升级版,两者在细胞与分子层面的本质是不同的。
我们需要从分子和细胞层面,加深对癌症转移的机制研究。通过精细对比两类癌细胞的生长代谢史,我们可以完成对杀手的详细的“犯罪侧写”。
只有知道癌细胞的个性与生活史,知道他们为什么流浪和怎样成功流窜,我们才可能真正克敌制胜。

尽管百年来我们一度对这些流浪杀手知之甚少,但是,现代生物学与医学的飞速发展让我们终于能一窥对手的手段。相信我们会越来越自信地面对再次狭路相逢。
其次,我们可以尝试改进传统的临床抗癌药物研究,给这些抗癌战士配置新的装备,按照各自能力下达新任务。
传统的抗癌药物临床试验主要针对原发性癌细胞,也就是比较安分的癌细胞。而这些战士能否抓到升级版癌细胞——流浪杀手,我们还不清楚。
例如,临床常用的贝伐珠单抗(Bevacizumab),在制服原发性癌细胞方面可以算是优秀的战士。
但是从部分试验来看,贝伐珠单抗对不同癌症类型,尤其是癌细胞转移的影响却不尽相同:面对不同的流浪杀手,这个抗癌小战士可能会失败,甚至有时叛变成为杀手的帮凶,协助杀手升级逃窜。
因此,对于传统抗癌斗士——抗癌药物与疗法来说,我们还需要考虑增加更多的考核标准,例如这些药物是否会刺激某些癌细胞“外逃”等等。同样的战斗人员,作战思路与策略不同,往往可以带来惊喜。
由于不同肿瘤多多少少共享同样的逃亡机制,针对肿瘤转移的治疗标准,不再仅仅是抑制肿瘤生长,更多是控制癌细胞转移机制。
转移过程涉及的多个步骤,包括自噬(autophagy)、上皮–间质转化(EMT)、失巢凋亡(anoikis)、细胞运动性(cell motility)以及肿瘤微环境(例如外排体)等都是目前各大药企和医学研发机构的重点靶标和具有前景的研究方向。
一些新型治疗手段,如微RNA(miRNA)、单克隆抗体(monoclonal antibody)、肿瘤新生抗原疫苗(neoantigen vaccine)、分子靶向治疗(molecularly targeted therapy)和抗体偶联药物(antibody-conjugated drug)则成为对抗癌症转移的核心技术。
这些新型治疗信息我们会在未来的日子里通过公众号向大家介绍。
最后,既然知道流浪杀手拥有更为狡猾的逃亡策略,那么实施抓捕的方案也需要及时更新。
我们需要开发新型的药物与治疗方案。比如筛选新型药物,防止潜在的“流浪杀手”们“离家出走”,又如在实验室里建立一套或多套针对癌细胞转移的新模型,让战士们化身“捕快”,有机会进行反复“实战演练”,从而达到防患于未然的效果。
实战中,面对癌症患者的治疗,我们需要更详细地考量癌症类型与转移风险大小,针对性地测试一些复合型的治疗方案。
换言之,如果单兵作战只能抓住原发性癌细胞,而控制不了转移性癌细胞,那么我们可以考虑派出一个联合部队,有的擅长狙击(靶向药),有的擅长格斗(化疗药),还有的擅长发动群众,对癌细胞群起而攻之(免疫疗法)。大家各取所长、协同作战,相信总有一天能让转移癌细胞销声匿迹。
当然,从患者的角度来说,与医疗机构的积极沟通,多方学习并参考专业意见,对于降低癌症转移风险也是至关重要的。更好地了解癌症类型、癌症转移的风险因子,与治疗团队咨询并探讨更合理的预防方案,是较为现实的。
一句话总结:早治疗,精准检查,多预防,达到在癌细胞出逃前就将其扼杀的效果。
记住两个关键词:
早——对原发肿瘤进行有效的治疗要趁早,及时阻断和抑制癌症的转移过程,孤立和限制其生长,将癌细胞就地正法。
准——制定更有效的,预测性更好的诊断标准。
如原发肿瘤治疗结束后,持续进行高解析度的影像学检查和血清学检查,采用更有效的病理推测方法,如生物标记物检测、肿瘤形态和生理学(淋巴结增大,浸润和病人生理状况)。
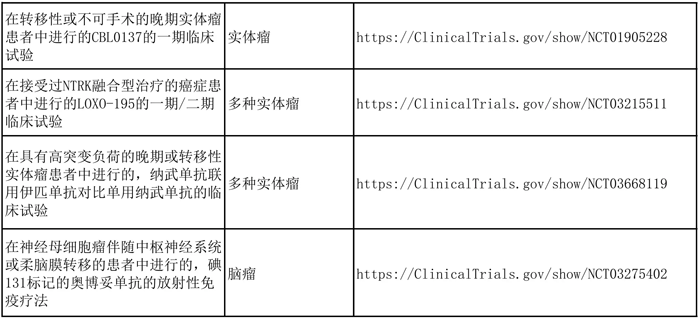
关注并参与目前针对癌症转移的临床研究,也是一个可行的路。针对目前世界上开展的收治儿童癌症转移患者的临床项目,我们收集了一些信息,供大家参考。
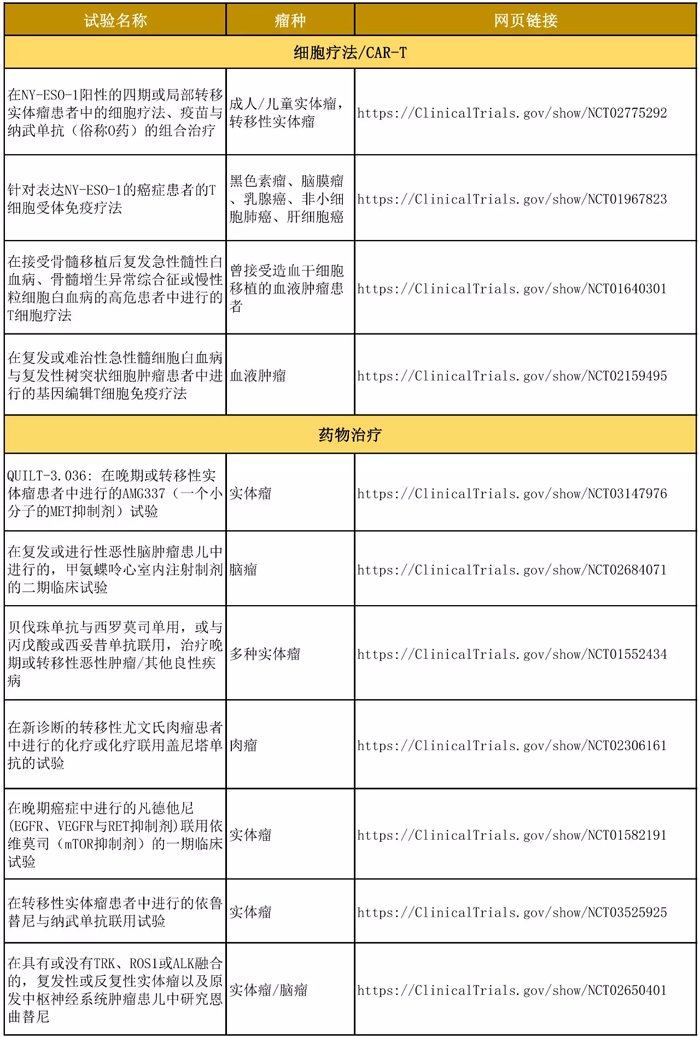
#在中国和欧盟的临床试验注册网站上,我们暂时没有找到合适的招募儿童癌症转移患者的临床试验。
有兴趣的读者可自行前往官网查询最新信息:
参考文献:
1. Paget S. The distrubition of secondary growths in cancer of the breast. Lancet 1889; 133: 571 – 573.
2. Anderson RL, Balasas T, Callaghan J, et al. A framework for the development of effective anti-metastatic agents. Nature Reviews Clinical Oncology 2019; 16: 185 – 204.
3. Hoshino A, Costa-Silva B, Shen TL, et al. Tumour exosome integrins determine organotropic metastasis. Nature 2015; 527 : 329 – 335.
4. Steeg PS. Targeting metastasis. Nature Reviews Cancer 2016; 16 : 201 – 218.
5. Kitamura T, Qian BZ, Pollard JW. Immune cell promotion of metastasis. Nature Reviews Immunology 2015; 15: 73 – 86.
6. Fernandez-Pineda I, Sandoval JA, Davidoff AM. Hepatic metastatic disease in pediatric and adolescent solid tumors. World Journal of Hepatology 2015; 7: 1807 – 1817.
7. Lambert AW, Pattabiraman DR, Weinberg RA. Emerging biological principles of metastasis. Cell 2017; 168; 670 – 691.
8. https://www.cancerquest.org/
9. http://www.childcancer.org.cn
✿
向大家介绍本期的几位作者!

周志诚
法国巴黎第五大学医学院内分泌、新陈代谢和癌症部研究员,研究方向为先天性糖尿病和自身免疫疾病。
爱好运动、旅游、摄影、写作和志愿者工作。加入向日葵儿童是一个偶然的机会又有其必然性。很高兴认识这里的志愿者小伙伴。期待向日葵儿童的发展有助于大家对中国儿童疾病的重视、预防和控制和全民儿童癌症科普教育。

高晓晖
耶鲁大学医学院博士后,研究方向为致病菌分子机制。希望通过加入向日葵儿童,在儿童癌症科普和治疗方面贡献力量。很高兴认识这里的志愿者小伙伴。

徐佳琳
先后求学于复旦与加拿大UBC,致力于研究遗传因素对个体的癌症易感性和抗癌药物安全性的影响。
很高兴能在向日葵儿童认识一群极其优秀、也充满抱负的志愿者们。经历十年癌症和衰老领域的临床和基础研究,我也真诚地希望能和大家携手,用我们的知识“兼济天下”——带癌症患儿和家属们走近科学,了解世界上最新的癌症研究进展。